水酸化アルミニウム沈殿 226435
Reaction formula aA bB = cC dD → Equilibrium constant K = C c D d / A a B b (β) When the relationship between the equilibrium constant (β) and each solute X is shown by the antilogarithm pX, it is shown by the following formula as the凝集沈殿法は水酸化アルミニウム表面 に砒素を吸着して共沈させ濾過分離する方法である。 第1図に水溶液のpHと砒酸種及びアルミニウム種の 関係を示す。アルミニウムイオンの加水分解過程で 燃焼排ガスの発生源としては、自動車等の移動発水酸化アルミニウムに関しては、もう一つ面白い性質があります。 図の左のように、アルミニウムイオンAl 3 が入った水溶液を用意しました。 この水溶液にNaOHを少量加えると、 Al(OH) 3 の沈殿が

高校化学 アンモニアと沈殿 映像授業のtry It トライイット
水酸化アルミニウム沈殿
水酸化アルミニウム沈殿-May 12, 21 · アルミニウムイオンと水酸化物イオンの沈殿反応 水溶液中で一定濃度範囲のアルミニウムイオンと水酸化物イオンが反応すると,不溶性の水酸化アルミニウムが沈殿します。 ※水酸化物イオンの濃度が高い場合,水酸化アルミニウムはテトラヒドロキシドαa=一L5×1061℃ αc=273×1c6/℃ 肇 であり12),そ の強度は本実験および従来の実験霊~3・13)から2500 ℃ までは増加し,そ れ以上ではやはりクリープのために強度が 著しく減ずることが知られている。 また弾性率も温度とともに上 10)FHGilley,EABush,ノノ1獅C加 辮Soo42,175 (1959) 11)EABush,FAHumme1,ノノ1粥α アσ獅Soo42, 3(1959)



Phと金属イオンの溶解度 水浄化フォーラム 科学と技術
したがって,過剰のアンモニア水を加えると,水酸化アルミニウムAl(OH) 3 が沈殿し,亜鉛はアンモニアの錯イオン,テトラアンミン亜鉛(II)イオンZn(NH 3 ) 4 2+ となって溶け,バリウムイオンは単原子イオンのままで水溶液中に存在します。アルミニウムイオンを含んだ水溶液に、塩基を加えると、水酸化アルミニウム Al (OH) 3 の白色ゲル状の沈殿が生じる。 水酸化アルミニウムを熱すると、酸化アルミニウム Al 2 O 3 が生じる。概要・一般的注意 赤色のアルミノンレーキの生成によって Al 3 を確認する(アルミノン反応).;
バイヤー法(バイヤーほう、英語 Bayer process )はアルミナ(酸化アルミニウム)の主要な工業的製造法である。 ホール・エルー法と併せ、アルミニウムの製造において重要である。 アルミニウムを含む主な鉱石であるボーキサイトは 40% から 60% しかアルミナ (Al 2 O 3) を含んでおらず、残りの>アンモニア水は触媒としてはたらいた。沈殿は水酸化アルミニウムal(oh)3で >発生した気体は水素h2でいいですか? 触媒として働くのはnh3なので「アンモニア『水』」ではなく「アンモニア」 です。Jun 29, 18 · Mg²⁺ 、 Al³⁺ 、 Zn²⁺ 、 Fe³⁺ 、 Fe²⁺ 、 Ni²⁺ 、 Sn²⁺ 、 Pb²⁺ 、 Cu²⁺ は水酸化物イオンと反応し、水酸化物が沈殿します。 マグネシウムイオンMg²⁺ Mg²⁺+2OH⁻→Mg(OH)₂↓(白) アルミニウムイオンAl³⁺ Al³⁺+3OH⁻→Al(OH)₃↓(白) 亜鉛イオンZn²⁺ Zn²⁺+2OH⁻→Zn(OH)₂↓(白)
水酸化アルミニウムに対するニyケJI,の共沈率と pHとの関係 3 1 A ニッケJI,の検量綜 25m!;)スプラスコ中に1x103M硫酸ニッケノレOlml2mlを採取し, OlM塩化アルミニヲム 10ml, 2M アンモニア~1((化アンモニクム125ml, 05% ゼラチ~05mlおよび水を加えて全容アルミニウムと硫黄との加熱により生成する。 2Al3S→Al 2 S 3 この反応では約1100℃の高温となり、鋼を溶かすほどである。冷却された硫化アルミニウムは非常に硬い。 空気中では、容易に加水分解をうけて、水酸化アルミニウムを沈殿させる。 脚注PACの主成分は、塩基性塩化アルミニウムで、一般式 Al 2 (OH) n Cl 6n m で示され、水溶液中ではアコ錯体 Al(H 2 O) 6 3 を有するばかりでなく、加水分解の過程で 種々の塩基性で、かつ 高い陽電荷を持つ多核錯体(ポリマー)を生成します。 一般に水処理の凝集過程では、凝集剤の添加により凝



水酸化アルミニウム 滴定曲線 溶解度などーエクセルを用いて




なぜ亜鉛がないと分かるのですか Clear
Dec 23, 11 · アルミニウムイオンを含む溶液に水酸化ナトリウムを加えるとまず Al^ (3) + 3OH^ → Al (OH)3 の反応により、Al (OH)3 <あなたの表現では" Al(H2O)3(OH)3"ですが一般的には略しますね>が沈殿します。標準水酸化アルミニウムsb92、b52は、酸、アルカリに対す る反応性、溶解性が優れているギブサイト結晶の湿粉で、硫 酸アルニウム、ポリ塩化アルミニウム、ゼオライトなど各種化 学製品に使用されます。sb93、b53は付着水分を除いた乾 粉です。(57)要約 本発明は、バイヤー法によるAl 2 O 3 の製造時に得られるアルミンン酸ナトリウムアルカリ液に基づいて、安定な水酸化アルミニウムゲルを製造する方法に関する。アルミンン酸塩を含むアルカリ液苛性モル比(遊離Na 2 O/Al 2 O 3 )は、1.6より小さく調節される。




水酸化礬土 181 ギトンの ギャるリ ど タブろ By ギトン Crooz Blog




水酸化アルミニウム沈殿物の意味 用法を知る Astamuse
Oct 05, · このアルミン酸ナトリウム溶液を冷やして、沈殿物(水酸化アルミニウム)を取り出す。 沈殿物を1,0℃以上で焼くことで、アルミニウムの酸化物であるアルミナ(Al2O3)ができる。Jan 24, 21 · 水酸化ナトリウム水溶液をアルミニウムイオンを含む水溶液に加えると沈殿(v) 水酸化アルミニウム Al(OH) 3 水酸化アルミニウム Al(OH) 3 は、酸を加えると中和されて溶解し、ヘキサアクアアルミニウムイオン Al(H 2 O) 6 3 となります。また、水酸化アルミニウム Al(OH) 3 は両性金属なので、水酸化ナトリウム NaOH 水溶液にも溶解し




粘土鉱物の化学 とやざき農園日誌



化学実験 Iii属 アルミニウム
ニウムを用いてホウ素を処理する場合、水酸化カル シウムの添加が必要不可欠であるということが明ら かとなった。カルシウムは水酸化アルミニウム沈殿 の見かけの比重を大きくして、凝集性、沈降性を高 めことが報告されている。さらに、過剰の硫酸イオAug 05, 18 · A)酸化アルミニウムに水酸化ナトリウム水溶液を加える Al 2 O 3 +2NaOH+3H 2 O→2NaAl(OH) 4 両性酸化物であるAl 2 O 3 は、HClなど酸とも反応(中和反応)し、塩基であるNaOHとも反応します。HClと反応する場合、Sep 25, 11 · 化学の問題です。化学反応式を教えてください。 硝酸アルミニウム水溶液にNaOHを加えると、白色沈殿が生じる。さらに、過剰のNaOHを加えると沈殿は溶ける。よろしくお願いします。 少量のNaOHで水酸化アルミニウムの白色沈殿ができる式Al(NO₃)₃3NaOH→Al(OH)₃3NaNO₃過剰のNaOHでテトラ




水酸化アルミニウムの沈殿に現れるスパイラルパターン Youtube



陽イオンの系統分離について質問です テトラヒドロキシドアルミ Yahoo 知恵袋
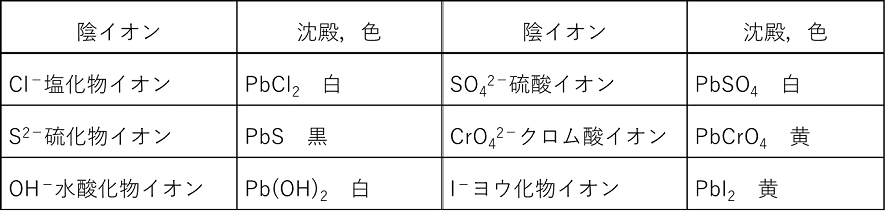
すいさんか‐アルミニウム〔スイサンクワ‐〕水酸化アルミニウム アルミニウム 塩類に アンモニア水 を加えて得られる白色の ゼラチン 状沈殿物。3 SO4によって沈殿するもの → アルカリ土類金属及びPb Ca2(CaSO4 白)、 Ba2(BaSO4 白)、 Pb2(PbSO4 白) ※ PbSO4 は鉛蓄電池の電極生成物でもある。 4 CrO42-(クロム酸イオン)によって沈殿するもの Pb2(PbCrO4 黄)、 Ba2(BaCrO4 黄)、 Ag(Ag2CrO4 暗赤色)は酸性を示し、水酸化ナトリウムや炭酸ナトリウム水溶液 などで中和すると水酸化アルミニウムの沈殿を生じる。そ の際コロイド状になっている水中の微細な濁りも取り込ま れるため、濁った水は短時間内に沈殿を生じ透明な上水が 得られる。



アルミニウムイオンは弱酸性にすると加水分解を起こして水酸化アルミニウムになる Yahoo 知恵袋




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット
水酸化カルシウムを水に溶かすと,(4)のように電離する. ca(oh) 2 →ca 2++2oh- (4) 水酸化カルシウムの飽和水溶液のphは124で,強アルカリ性である. 一方,リン酸は3価の酸であり,以下のように3段階に電離する5). h 3po 4 →h ++h 2po 4 - pk a1 =1 (5) h 2poMay 14, 19 · しかしながら、沈殿後時間が経過したものおよび、結晶性の水酸化アルミニウムは特に塩基水溶液に対し溶解しにくくなる。塩化アルミニウムと水酸化ナトリウムの沈殿反応で生成される 2種類の沈殿物 作者 藤田清菜 末松 j信彦 作者机构 明大総合数理,明大総合数理 会议名称 日本化学会春季年会講演予稿集 会议地点 神戸 会议时间 会议录名称



無機化学 イオンの系統分離




陽イオンの系統分析の問題です Clear
水酸化アルミニウム(すいさんかアルミニウム、Aluminium hydroxide)は化学式 Al(OH) 3 で表される無機化合物である。 比重は約242。 酸やアルカリに溶け、水、アルコールに不溶。 アルミニウム 塩の水溶液にアンモニアを加えると白色ゲル状沈殿を起こすが、これが水酸化アルミニウムである。単体金属の製造はまず原料であるボーキサイトに熱濃水酸化ナトリウム水溶液を反応させてアルミン酸ナトリウムとして溶出させ、希釈して沈殿する水酸化アルミニウムAl(OH) 3 を焼成してアルミナAl 2 O 3 を得る。このアルミナを氷晶石と混ぜ1000℃で融解し水酸化アルミニウムに対する銅の共沈 143 沈殿中の銅の定量には,ヨワ素法またはポーラログラブ法を用いた口すなわち,沈殿を酢酸に溶 解したのち,チオ硫酸ソーダ標準溶液で滴定する方法または,沈殿を過塩素酸に溶解しlN過塩素




0100 Ai3 A Bardfractt1 A Descubre Como Resolverlo En Qanda




沈殿生成反応 化学がちょっとだけ好きな社労士
やがて一定量に達し,水酸化アルミニウムの沈殿が 100 %に 達したのち,さ らに尿素を加えて反応を継続しても 硫酸イオンの共沈殿量は増加しないす なわち,硫 酸イ オンは水酸化アルミニウムが沈殿しつつある場合にのみH2S ⇄ 2H+ + S2- K=H+2S2-/ H2S= 12×10-21(mol/L)2 これより,S2- = 12×10-21H2S/H+2 ≒ 12×10-22/H+2 pH=10の場合は,H+=10×10-1より,S2- = 12 × 10- 。 pH=50以上では,計算上S2-は01〔mol/L〕を超え,完全に電離していると考えられるのでS2-=01。32 酸化物やケイ酸塩の溶解・沈殿反応 地球表層を構成する鉱物のほとんどは酸化物、水酸化物およびケイ酸塩鉱物 単一の金属からなる酸化物、水酸化物およびケイ酸塩鉱物 石英SiO 2、アモルファスシリカSiO 2、 ヘマタイトFe 2O



Phと金属イオンの溶解度 水浄化フォーラム 科学と技術



放課後化学講義室 意外な塩化アルミニウム




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット




水酸化ナトリウムとアンモニアで 同じものが沈殿してるけど上に沈殿してるのと下に沈殿す Clear



硝酸アルミニウム Aluminium Nitrate Al No 3 3 9h 2 O D G Cm 3 Mp 73ºc Bp ºc
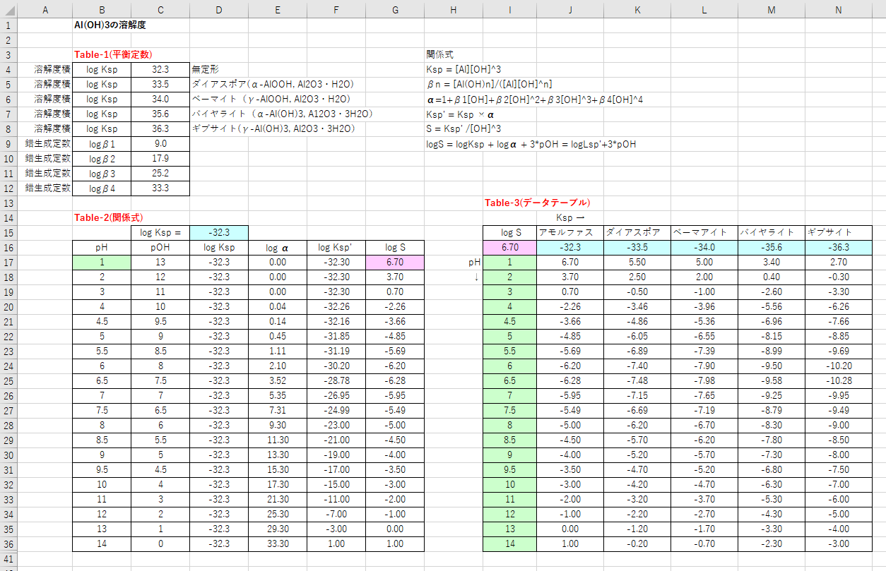



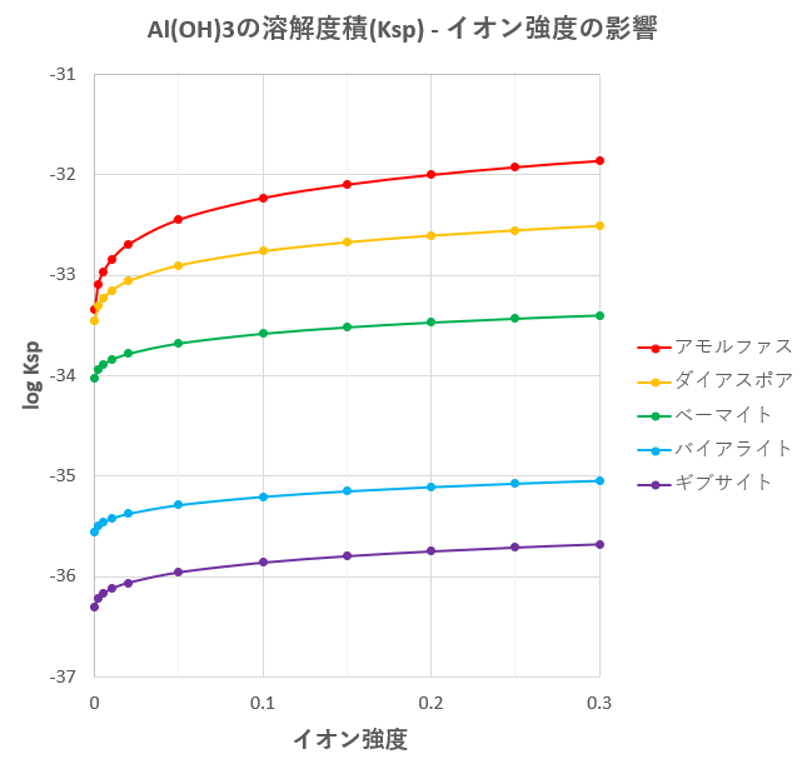
水酸化アルミニウムの溶解度に及ぼす影響 その1 結晶形 滴定曲線 溶解度などーエクセルを用いて




4 Ahc1 Lihat Cara Penyelesaian Di Qanda



化学実験 Iii属 アルミニウム




7fxbja D Y58dm




水酸化アルミニウム Wikiwand




伊藤忠ケミカルフロンティア 新卒採用サイト ビジネスフィールド



無機化学 沈殿生成反応




13 号 A 酸化アルミニウム前駆体ゾル その製造方法 及びイットリウム アルミニウム ガーネットの製造方法 Astamuse




水酸化アルミニウムの沈殿に現れるスパイラルパターン Youtube




語呂合わせと徹底整理で攻略する高校無機化学 両性元素 水銀 合金篇 永野裕之のblog




重金属を含んだ排水の処理方法 水処理に関するご相談は 栗田工業




問題aについてなんですが ボーキサイトは一般にal2o3 Nh2oで表されることが多 Clear




高校化学 アルミニウム化合物の性質 練習編 映像授業のtry It トライイット



Phと金属イオンの溶解度 水浄化フォーラム 科学と技術




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット
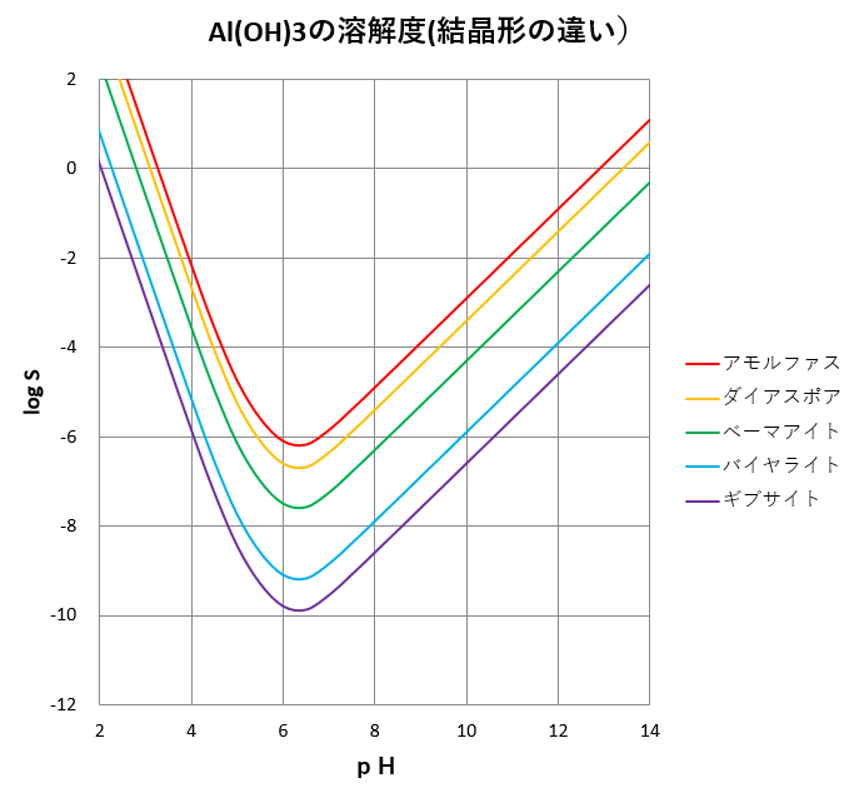



水酸化アルミニウムの溶解度に及ぼす影響 その1 結晶形 滴定曲線 溶解度などーエクセルを用いて



化学実験 Iii属 アルミニウム



水酸化亜鉛に過剰のアンモニア水を加えたらできるのはテトラアンミン亜鉛 イ Yahoo 知恵袋




水を徹底的に浄化 株式会社 ナカテック



硫酸アルミニウム水溶液に水酸化ナトリウム水溶液を少しずつ 最終的に Yahoo 知恵袋




陽イオンの系統分析についてです 問5の解き方を教えてください ちなみに答えは D Clear
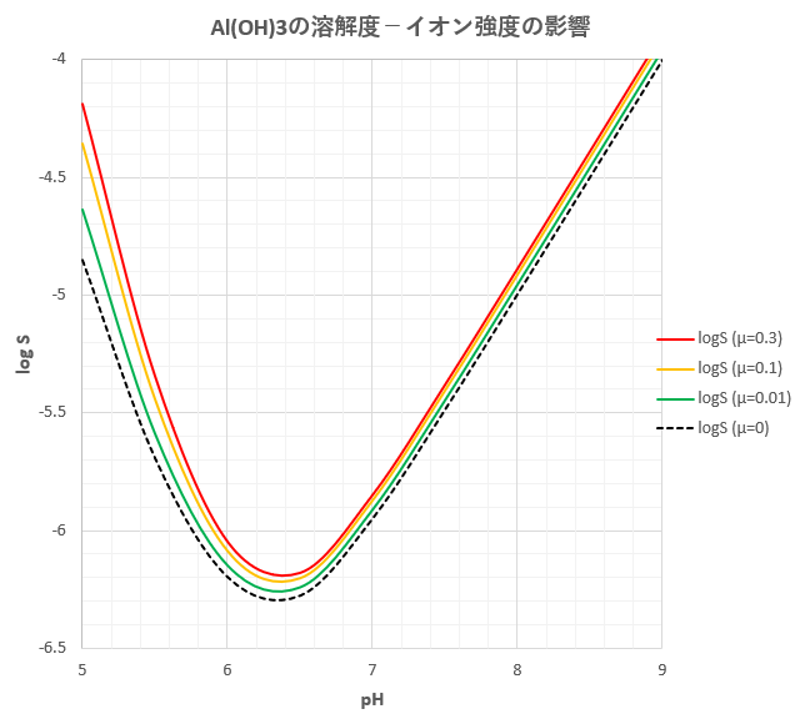



水酸化アルミニウム 滴定曲線 溶解度などーエクセルを用いて




51 2 水酸化アルミニウムゲル Aluminium Hydroxide Gel 012 詳細情報 ライフサイエンス 試薬 富士フイルム和光純薬




51 2 水酸化アルミニウム Aluminium Hydroxide 014 詳細情報 試薬 富士フイルム和光純薬




水酸化アルミニウム沈殿物の意味 用法を知る Astamuse




07 3793号 水酸化アルミニウムの製造方法およびその装置 Astamuse



第55章 実験 アルミニウムと亜鉛




Lihat Cara Penyelesaian Di Qanda




水酸化礬土 181 ギトンの ギャるリ ど タブろ By ギトン Crooz Blog




水酸化ナトリウムは強塩基でアンモニアは弱塩基になるため 沈殿が生じないと考えて1番を Clear
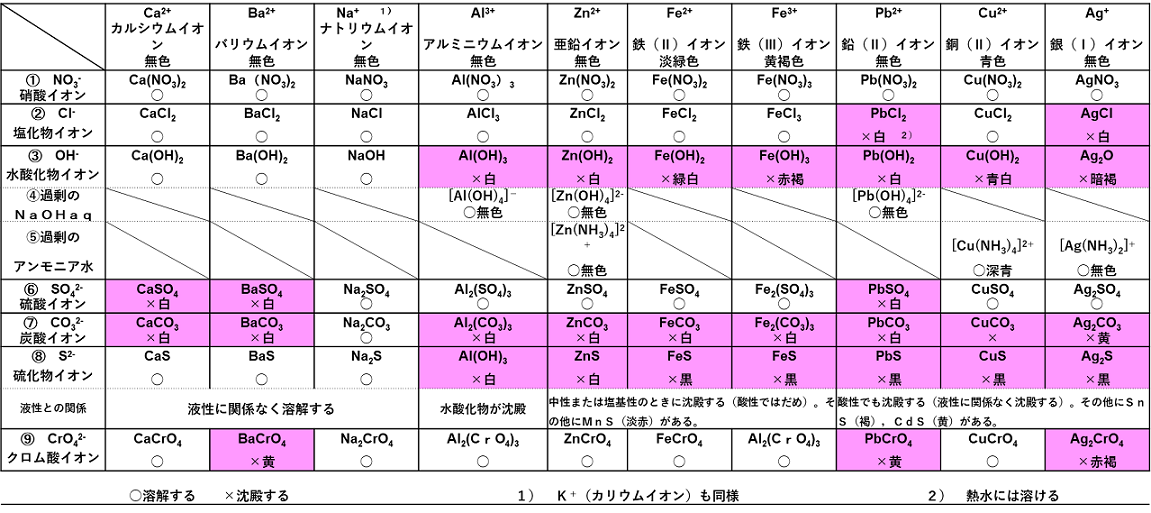



金属イオンの沈殿反応



化学です 写真の問題でアンモニア水を加えた時になぜアルミニウムだけが沈殿 Yahoo 知恵袋




9 O Times Left Vec7 Righ Lihat Cara Penyelesaian Di Qanda



水酸化酸化アルミニウムの変換のための方法




51 2 水酸化アルミニウム Aluminium Hydroxide 014 詳細情報 試薬 富士フイルム和光純薬




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット




高校化学 アンモニアと沈殿 映像授業のtry It トライイット



第13族元素 ホウ素族元素




B B Lihat Cara Penyelesaian Di Qanda



イオン ナトリウム 沈殿物 水酸化アルミニウム 化学 分析 アルカリ性 の画像素材 写真素材ならイメージナビ




センター試験対策 アルミニウムに関する問題 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc




1999 号 結晶性水酸化アルミニウムの製造方法 Astamuse



化学実験 Iii属 アルミニウム
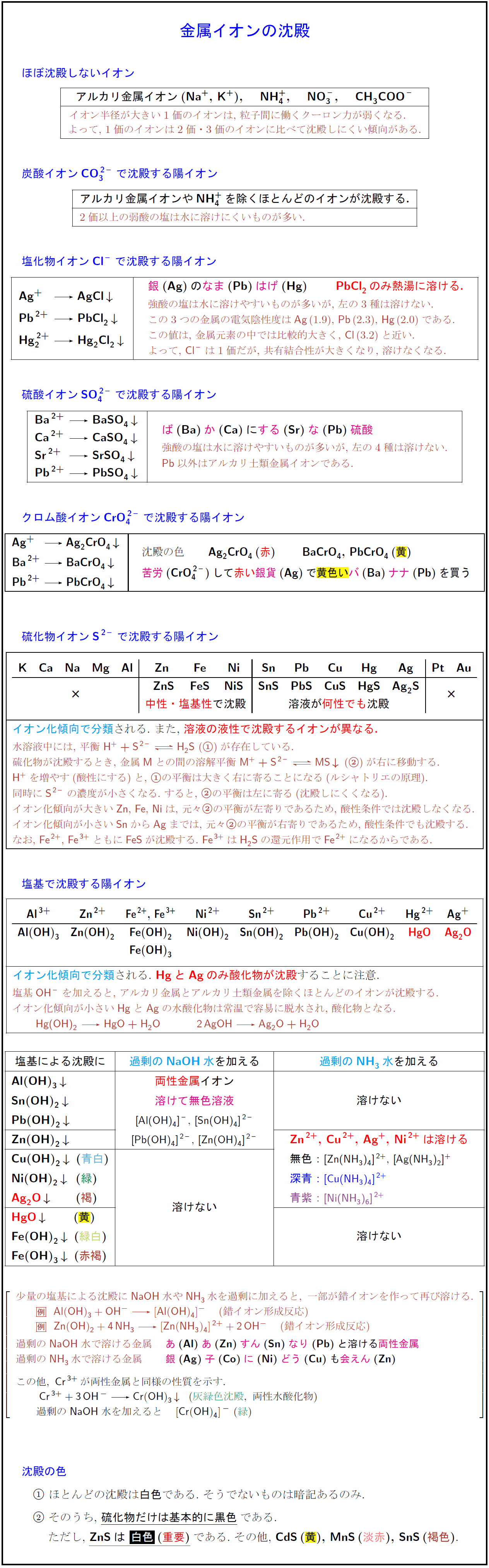



高校無機化学 金属イオンの沈殿まとめ 金属元素最重要事項 受験の月



第55章 実験 アルミニウムと亜鉛



第54章 アルミニウムと亜鉛



化学実験 Iii属 アルミニウム




1996 号 水酸化アルミニウムの白色度を改良する方法 Astamuse



中国難燃剤 肥料 水酸化アルミニウムサプライヤー 製造 工場 Elite




汚水処理の凝集沈殿の原理 Aktio アクティオエンジニアリング事業部



A 酸化アルミニウム前駆体ゾル その製造方法 及びイットリウム アルミニウム ガーネットの製造方法



化学実験 Iii属 アルミニウム




くまぐま なちゅ



放課後化学講義室 意外な塩化アルミニウム




12 号 水酸化酸化アルミニウムの変換のための方法 Astamuse



化学実験 Iii属 アルミニウム



なぜ水酸化鉄や水酸化アルミニウムはゲル状沈殿を生成するのでしょうか 詳しく Yahoo 知恵袋




11 1347号 低級炭化水素直接分解用触媒の製造方法 Astamuse



Phと金属イオンの溶解度 水浄化フォーラム 科学と技術
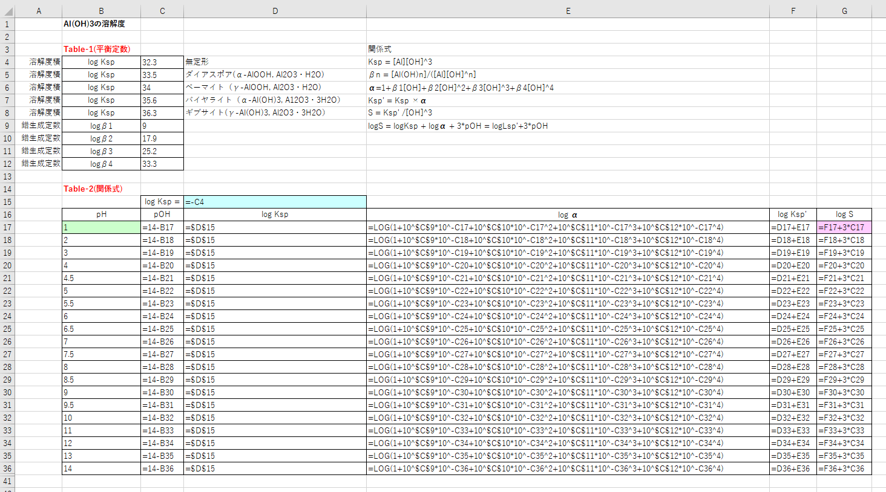



水酸化アルミニウムの溶解度に及ぼす影響 その1 結晶形 滴定曲線 溶解度などーエクセルを用いて
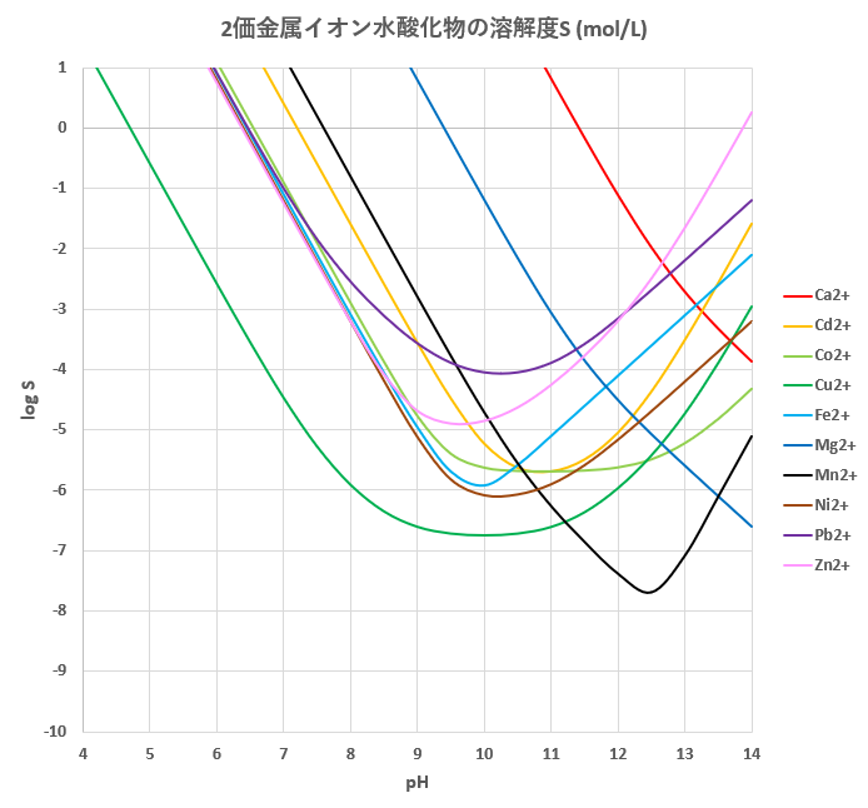



年01月 滴定曲線 溶解度などーエクセルを用いて




理科とか苦手で アルミ箔で銅の廃液処理 後編




アルミニウムイオンと硫化水素の反応の所が斜線になっているのはなぜですか Clear
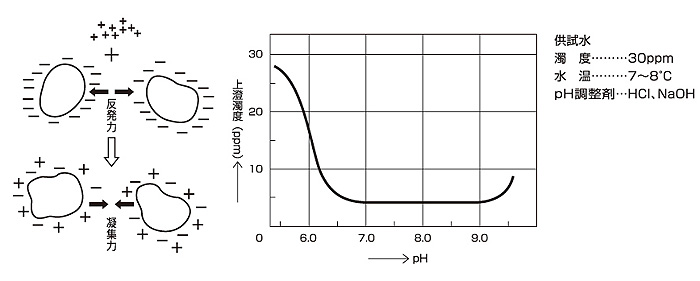



汚水処理の凝集沈殿の原理 Aktio アクティオエンジニアリング事業部




無機凝集剤 朝日化学




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット




Asnr プリント黒板実験映像8 水酸化アルミニウムの生成 Youtube
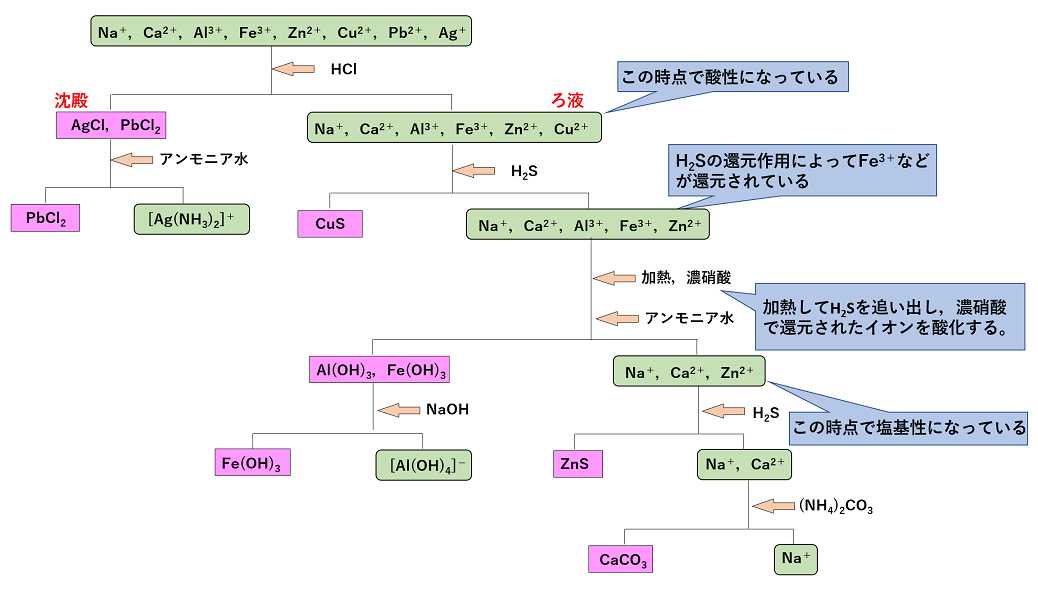



金属イオンの沈殿反応




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット




アルミニウムイオンと亜鉛イオンの違い Youtube
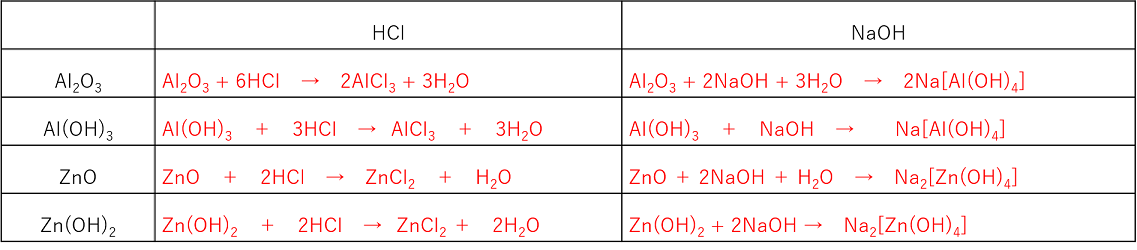



アルミニウム 亜鉛 スズ 鉛 水銀
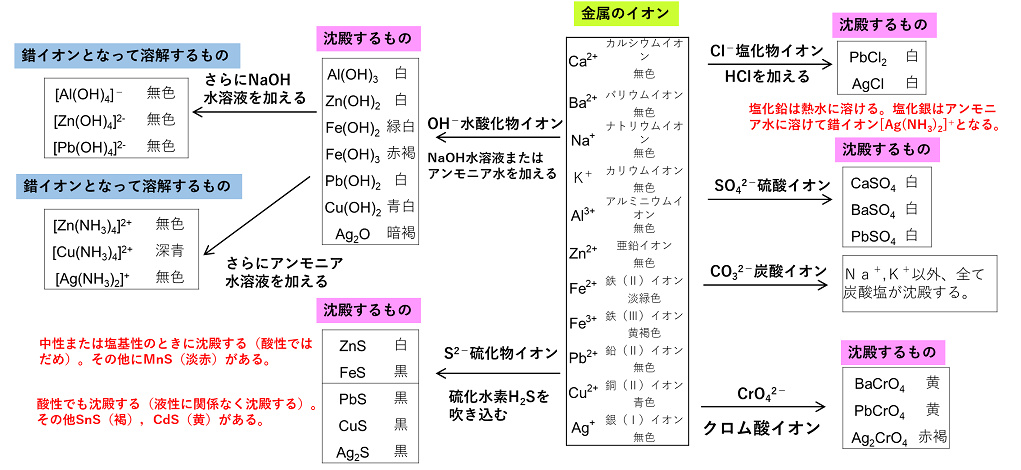



金属イオンの沈殿反応




金属イオンの分離 系統分析実験しました その2 なんとなく実験しています



アルミニウム 亜鉛 スズ 鉛 水銀
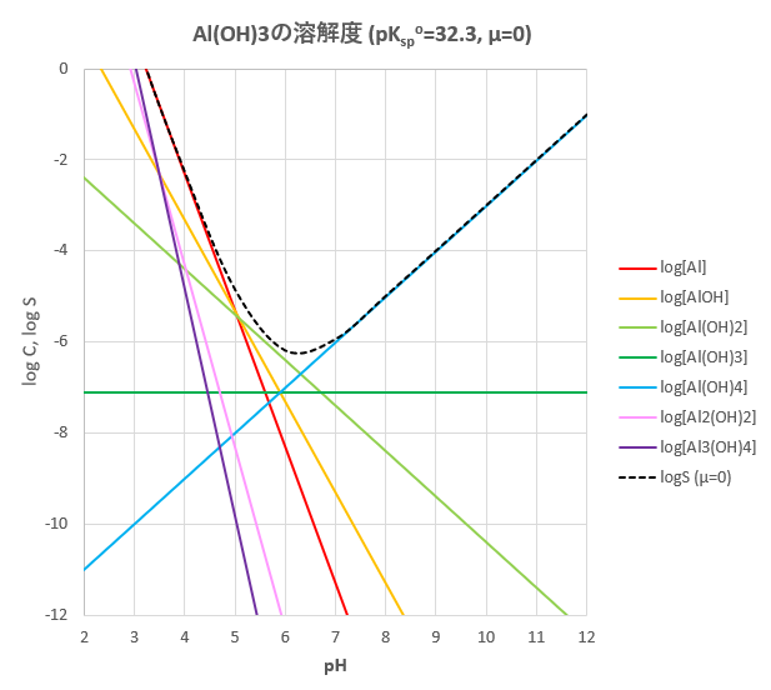



水酸化アルミニウムの溶解度に及ぼす影響 その3 多核錯体 滴定曲線 溶解度などーエクセルを用いて



Al3 に塩基性硫化水素をぶちこむとき水酸化アルミニウムが生じる Yahoo 知恵袋




Japaneseプレイヤーの販売 オンラインショッピング アルミナ水和物 Alibaba Comでのjapaneseプレイヤーの販売
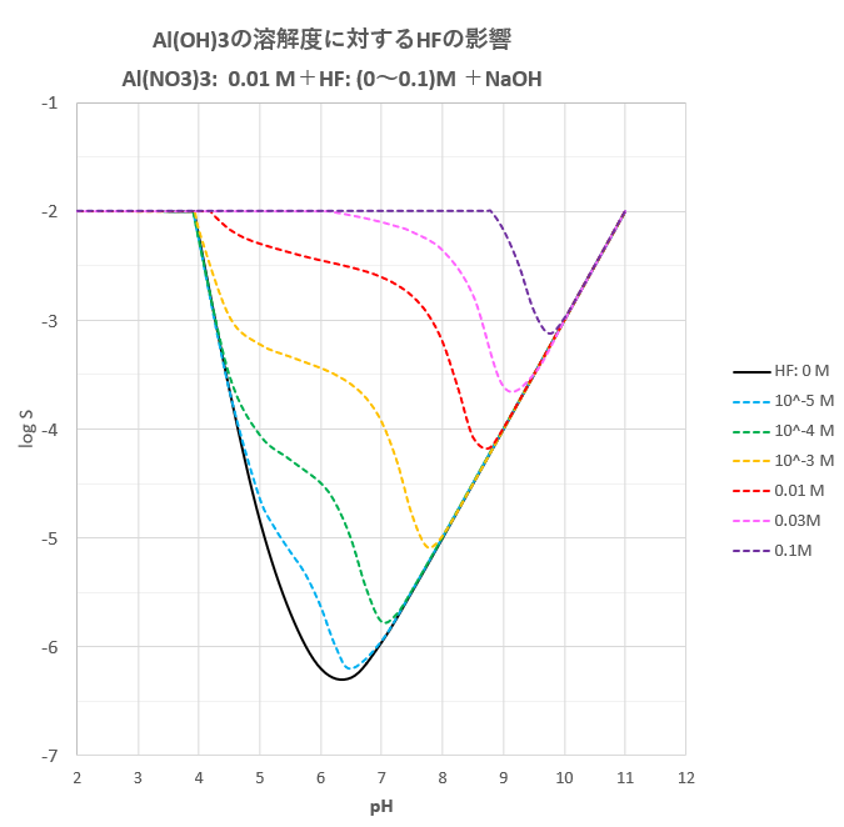



水酸化アルミニウムの溶解度に及ぼす影響 その4 錯形成剤の添加 滴定曲線 溶解度などーエクセルを用いて




アルミニウム の特徴と製法について元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン



第55章 実験 アルミニウムと亜鉛



コメント
コメントを投稿